|
|

|
|
ASÍ FUNCIONAN LOS ÁTOMOS
Texto e ilustraciones José Antonio E. García Álvarez
|
|
|
|
Un átomo simple de un mismo elemento constituye, a su vez, una molécula simple del propio elemento. El oxígeno (O), hidrógeno (H), cloro (Cl), sodio (Na), cobre (Cu), hierro (Fe), plata
(Ag) y el oro (Au), por ejemplo, son átomos de elementos
simples y constituyen, al mismo tiempo, moléculas de cada uno de esos mismos elementos..
|
|
|
 |
|
|
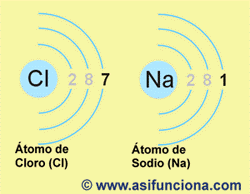
Átomo de cloro (Cl), cuyo número atómico es 17, de acuerdo con la suma total de electrones que posee. en sus tres órbitas
(2 + 8 + 7 = 17) y átomo de
sodio (Na), de número atómico 11, de acuerdo también. con la suma de la
cantidad de electrones que posee (2 + 8 + 1 = 11). Como se puede apreciar, el cloro. posee 7
electrones en su última órbita, por lo cual es más propenso a captar el
electrón que le falta para. completar ocho, mientras que el sodio, al tener sólo 1 electrón, es más
propenso a cederlo.
|
Iones positivos y negativos
|
|
Normalmente un átomo mantiene carga eléctrica neutra mientras no se altere el balance existente entre la cantidad de electrones con carga negativa girando en su última órbita y la cantidad de protones con carga positiva contenidas en el núcleo. Sin embargo,
ese balance se puede alterar si excitamos el átomo mediante la aplicación de calor, luz,
corriente eléctrica o por medio de una reacción química. Con
alguno de esos métodos un átomo puede ganar o ceder uno o varios electrones en
su última órbita y convertirse en un ión del propio elemento químico.
Así, cuando el átomo cede o pierde electrones, se convierte en un ión positivo o “catión” del elemento
de que se
trate, debido a que en esa situación la carga eléctrica positiva de los protones
del núcleo
supera a la negativa de los electrones que quedan girando en sus respectivas órbitas.
En el caso contrario, cuando el átomo gana algún electrón en la última órbita, se convierte en un ión negativo o “anión”, pues
en ese caso la carga eléctrica negativa
(–) de los de electrones superará a la carga positiva de los protones contenidos en el núcleo.
Tanto los iones positivos como los negativos, son los responsables de que los átomos
manifiesten fenómenos físicos y reacciones químicas.
|
|
|
 |
|
|
Un átomo de cloro cuando se enlaza con otro de sodio gana un electrón en su última
órbita, completando. ocho electrones. Así se convierte
en un ión negativo o anión cloro (Cl –),
pues la suma total de< electrones con carga negativa supera a la de protones con carga positiva
contenidos en su núcleo. El. átomo de sodio, por su parte, al cederle al cloro en
ese enlace el único electrón que posee en su última. órbita, se convierte en un ión positivo
o catión sodio (Na +), pues en este caso la carga positiva de los. protones
contenidos en el núcleo supera a la suma total de los electrones que han quedado girando en
el. resto de.sus órbitas.
|
|
Cuando el ión de un elemento simple se combina con uno o más iones de otros elementos simples diferentes, se obtiene una sustancia compuesta. Si combinamos un átomo de oxígeno (O) con dos de hidrógeno (H) (tanto uno como el otro en estado natural son gases), obtendremos un elemento compuesto, con características completamente diferentes, en este caso “agua” (H2O);
es decir, combinando dos gases se ha obtenido un líquido.
|
Por otra parte, si combinamos una molécula de
Cloro (Cl) con una de sodio (Na), obtendremos una molécula de “cloruro
de sodio” (Cl Na), compuesto comúnmente conocido como “sal común”, con
características completamente diferentes a los dos elementos simples que le
dieron origen.
Cl– + Na+ = Cl
Na
|
|
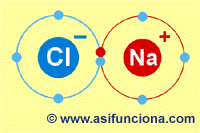
Molécula de Cloruro de Sodio o< sal común.
|
|
Se pueden combinar también más de dos moléculas o átomos diferentes para obtener compuestos químicos más complejos. Por ejemplo,
si combinamos dos moléculas de hidrógeno (H2), una de azufre (S),
más cuatro de oxígeno (O4), obtenemos H2SO4, o lo que es lo mismo, “ácido sulfúrico”, compuesto químico
altamente corrosivo y muy utilizado en las baterías de
los vehículos automotores.
|
|
|

