|
|

|
|
ASÍ FUNCIONAN LOS ÁTOMOS
Texto e ilustraciones José Antonio E. García Álvarez
|
|
|
ENLACES QUÍMICOS ENTRE ÁTOMOS
|
|
Los enlaces químicos entre los átomos de los elementos se efectúan en estrecha relación con la cantidad de electrones que posean en la última órbita. Esa cantidad de electrones determina
el número de valencia o de oxidación con la que los átomos realizan los
enlaces químicos.
Se denomina banda de valencia al último nivel de energía u
órbita más alejada del núcleo del átomo, donde se efectúan
las combinaciones químicas. La banda de valencia permite que los electrones que
giran en la última órbita puedan pasar de un átomo a
otro, en dependencia de su "número de valencia" o "número de
oxidación", que puede
ser positivo (+), o negativo (–), de acuerdo con las propiedades específicas de cada
elemento en cuestión. Así, según sea la electronegatividad o
tendencia que tenga el átomo de una molécula para atraer electrones de acuerdo
con su número atómico o valencia, se forman iones positivos o
negativos.
En la siguiente tabla se presentan algunos elementos químicos
con su respectivo número atómico, número o números de oxidación o
valencias y la cantidad de electrones que poseen en cada nivel
de energía. Como se podrá apreciar el Neón (Ne) no posee
número de valencia por ser éste un gas noble o inerte. Todos los
gases de ese tipo contienen el máximo de electrones posibles
en el último nivel de energía, o sea, ocho, por lo cual
ninguno de ellos reaccionan químicamente con otros elementos.
Además del Neón, entre los gases inertes se encuentran
también el helio (He), argón (Ar), kriptón (Kr), xenón
(Xe) y el radón (Rn).
|
| Elemento |
Símbolo químico |
Número atómico |
Número de oxidación o valencia |
Cantidad de electrones por nivel de energía |
| Hidrógeno |
H |
1 |
+1, -1 |
1 |
| Oxígeno |
O |
8 |
-2 |
2 – 6 |
| Neón |
Ne |
10 |
No tiene |
2 – 8 |
| Sodio |
Na |
11 |
+1 |
2 – 8 – 1 |
| Silicio |
Si |
14 |
-4, +2,
+4 |
2 – 8 – 4 |
| Cloro |
Cl |
17 |
-1, +1,
+3, +5 , +7 |
2 – 8 – 7 |
| Hierro |
Fe |
26 |
+2, +3 |
2 – 8 – 14 – 2 |
| Cobre |
Cu |
29 |
+1, +2 |
2 – 8 – 18 – 1 |
| Plata |
Ag |
47 |
+1 |
2 – 8 – 18 – 18 – 1 |
| Oro |
Au |
79 |
+1, +3 |
2 – 8 – 18 – 32 – 18 – 1 |
Diferentes tipos de enlaces
|
Los diferentes tipos de enlaces químicos que ocurren entre átomos de
elementos simples son los siguientes:
|
|
|
|
Enlace iónico o electrovalente.
Debido a la fuerza
de atracción que se ejerce entre los iones con cargas de signo contrario
(positivas y negativas), se originan enlaces iónicos o electrovalentes, que dan
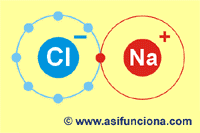
lugar a la creación de moléculas de elementos químicos compuestos. Por ejemplo, las cargas de un ión cloro negativo (Cl–)
o anión y la de un ión sodio positivo (Na+) o catión, se atraen mutuamente para dar lugar a la formación de una molécula de cloruro de sodio,
más conocida como sal común (NaCl). |
|
|
|
|
|
Enlace electrovante o iónico entre. un ión cloro (Cl -) y un
ión sodio. (Na +).
|
|
|
|
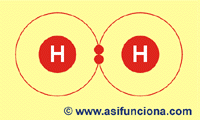
Enlace covalente. Ocurre cuando dos átomos comparten sus electrones como, por ejemplo,
cuando se unen dos moléculas de hidrógeno (H + H = H2)
u otros elementos similares, como el nitrógeno (N2), oxígeno
(O2),
cloro (Cl2), etc.
|
|
Enlace covalente entre dos átomos de hidrógeno (H2).
|
|
Enlace metálico. Se efectúa cuando los electrones que se encuentran girando en la última órbita de los átomos de un metal se mueven por una estructura molecular, manteniéndola unida
como ocurre, por ejemplo, con el cobre: Cu
|
|
|

